I. Pendahuluan: Simtom, Faktor, dan Epidemiologi dari Artritis Reumatoid
Artritis reumatoid (Rheumatoid Arthritis, RA) adalah penyakit infalamsi kronis autoimun yang paling umum ditemukan (Smolen et al., 2016). RA paling banyak menyerang persendian (artikulasi) dan bersifat long term (Smolen et al., 2016). RA menyebabkan inflamasi pada membran sinovial persendian sehingga menyebabkan persendian tersebut menjadi membengkak dan kaku. Hal ini dapat menyebabkan rasa sakit yang luar biasa pada sendi dan kekakuan sendi menyebabkan terbatasnya pergerakan anggota badan (CDC, 2018). Dalam jangka waktu yang lama, RA dapat menyebabkan degradasi tulang rawan dan erosi pada tulang (McInnes & Schett, 2011). Selain itu, pembengkakan sendi karena RA dapat menyebabkan hilangnya keseimbangan pada tubuh dan dapat menyebar ke organ lain seperti paru-paru, jantung, dan mata (CDC, 2018).
Simtom dari penyakit RA cukup beragam, meliputi rasa sakit pada sendi, kekakuan pada sendi, pembengkakan pada sendi, naiknya suhu pada sendi, demam, rasa lelah luar biasa, dan penurunan berat badan (CDC, 2018). Individu yang terkena penyakit RA dilaporkan mengalami penurunan fungsi fisik, penurunan kualitas hidup, penurunan produktivitas ekonomi, penurunan partisipasi dan interaksi sosial, serta berkurangnya jam kerja (Smolen et al., 2016)s. Hal ini tentu saja mempengaruhi sosioekonomi penderita RA.
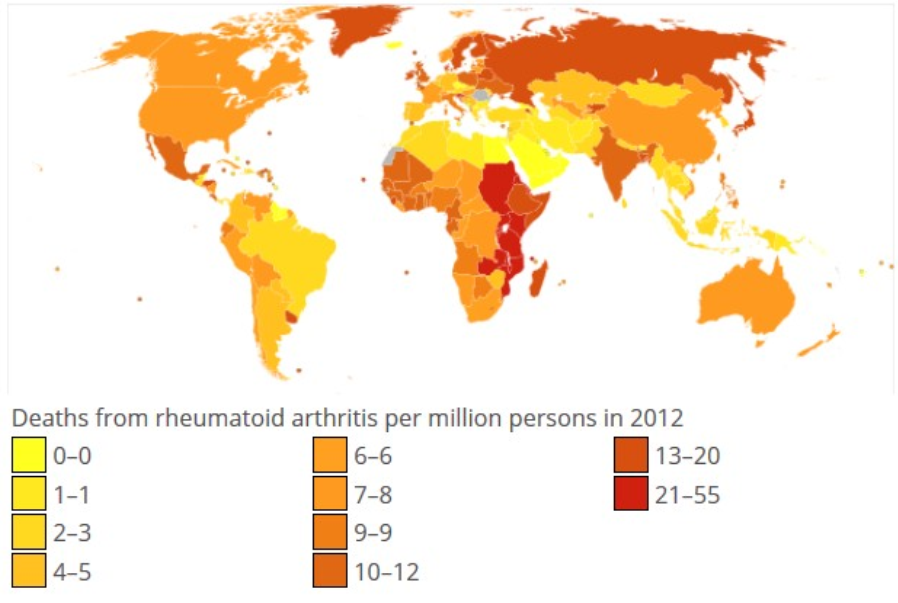
Secara epidemiologi (distribusi penyakit), RA adalah penyakit yang sangat umum dijumpai di dunia. Tingkat kematian akibat RA adalah sebanyak 1 hingga 55 kematian per juta orang pada tahun 2012 (WHO, 2012). RA menyerang 0.5% hingga 1% dewasa di negara-negara berkembang. Selain itu, lima hingga lima puluh orang tiap 100,000 individu terkena RA tiap tahunnya (Smolen et al., 2016). Secara umum, gejala RA meningkat ketika usia semakin tua, dimulai dari gejala awal pada usia sedini 15 tahun dan semakin meningkat seiring usia hingga 80 tahun (Shah, 2012). Data juga menunjukkan bahwa perempuan tiga hingga lima kali lebih rentan terkena RA daripada laki-laki (Shah, 2012). Data-data epidemiologi juga menunjukkan bahwa RA adalah penyakit yang umum dijumpai dan menyebar di seluruh dunia (Gambar 1).
Di lain sisi, penyebab penyakit RA belum diketahui secara utuh. Banyak dari penyebab RA yang masih belum dapat ditentukan. Meski begitu, beberapa mekanisme pembentukan RA telah diteliti. Namun, menurut McInnes & Schett (2011), beberapa terapi masih gagal dalam menunjukkan hasil positif pada pasien pengidap RA. RA juga dilaporkan menginduksi penyakit sistemik. Penyakit RA bukanlah penyakit lokal yang menyerang pada sendi saja, namun dapat berhubungan dengan organ lain dan seluruh sistem tubuh (McInness & Schett, 2011).
Faktor-faktor yang menyebabkan RA bermacam-macam, mulai dari faktor lingkungan dan genetik. RA adalah penyakit terturunkan dengan derajat heratibilitas sekitar 40-65% untuk RA seorpositif (Smolen et al., 2016). Terdapat beberapa lokus gen di dalam kromosom manusia yang memiliki asosiasi dengan RA. HLA-DRB1 adalah salah satu lokus yang dapat menginduksi inflamasi kronis dan berpengaruh terhadap peningkatan risiko RA (Smolen et al., 2016). Selain itu, CTLA4, CD28, IL21 IL2RB, CD40, PTPN22, IL6R, IRAK1, dll. (Gambar 2) juga merupakan lokus yang berasosiasi dengan penyakit RA. Umumnya, lokus-lokus di atas mengubah stimlulatory pathway dari aktivasi sistem imun, termasuk signalling sitokin dan aktivasi reseptor limfosit (Smolen et al., 2016). Seperti yang telah dijelaskan di atas, RA termasuk ke dalam penyakit autoimun, yaitu keadaan ketika imun tubuh sendiri (self immune) menyerang dirinya sendiri (sel dan jaringan di sekitarnya).

Selain faktor genetik, faktor lingkungan diketahui memiliki asosiasi dengan peningkatan risiko RA (Smolen et al., 2016). Faktor-faktor tersebut meliputi aktivitas merokok, status sosioekonomi yang rendah, dan rendahnya tingkat pendidikan. Selain itu, kondisi mikrobioma di saluran pencernaan juga diduga memiliki hubungan kausalitas dengan RA. Gastrointestinal dysbiosis dapat menyebabkan RA tahap awal, sedangkan perubahan komunitas mikrobioma di dalam mulut, saliva, dan saluran pencernaan juga memiliki asosiasi dengan RA (Smolen et al., 2016). Mekanisme mikrobioma dan hubungannya dengan RA belum diketahui secara pasti, akan tetapi, mekanisme dari sistem imun telah diketahui dengan cukup detail.
II. Patofisiologi dan Patogenesis Artritis Reumatoid
RA umumnya diawali oleh berbagai jenis mekanisme selular yang berujung pada autoimunitas di sekitar sendi dan organ-organ lainnya. Fase awal RA terjadi ketika membran sinovial di sendi diinfiltrasi oleh sel-sel imun dan terdapat inflamasi non-spesifik di situs tersebut. Sebelum fase awal terjadi, sebenarnya terdapat berbagai event yang berujung pada dimulainya fase awal RA.

Di sini, saya akan membaginya dalam empat event(Gambar 3). Yang pertama adalah pra-artritis. Di pra-artritis terjadi berbagai faktor yang mengarah ke pemebentukan RA (Smolen et al., 2016). Meski belum terjadi RA, fase pre-artritis adalah fase terpenting sebab di fase inilah RA sedikit demi sedikit mengalami progresi. Faktor-faktor tersebut adalah faktor genetik, faktor lingkungan, modifikasi epigenetik, dan modifikasi post-translasi (Smolen et al., 2016). Dua faktor pertama (faktor genetik dan faktor lingkungan) telah saya jelaskan di atas. Faktor epigenetik seperti adanya deasetilasi histon dan modifikasi post-translasi seperti asetilasi, karbamilasi, metilasi dan fosforilasi protein, bersamaan dengan faktor genetik dan faktor lingkungan, dapat menyebabkan hilangnya toleransi sistem imun (Smolen et al., 2016).
ACPA (anti-citrullinated protein antibodies) adalah autoantibodi yang mengenali dan melawan peptida atau protein yang tersitrulinasi. Pasien penderita RA memiliki kadar ACPA yang lebih tinggi daripada normal. Ketika inflamasi, asam amino arginin dapat terkonversi menjadi sitrulin. Proses ini disebut sebagai sitrulinasi. Proses sitrulinasi menyebabkan struktur tiga dimensi protein menjadi berubah. Hal ini menjadikan tubuh menganggap protein tersitrulinasi sebagai antigen, sehingga menghasilkan sebuah respons imun (Raptopoulou et al., 2007). ACPA dapat berikatan dengan self-protein dengan residu sitrulin seperti vimentin, fibronectin, fibrinogen, histon, dan kolagen tipe II (Smolen et al., 2016).
Mengapa pasien RA memiliki ACPA lebih tinggi dari normal? Kembali lagi ke faktor genetik, bahwa individu yang memiliki lokus HLA-DRB1 yang menginduksi pelepasan ACPA dan meningkatkan risiko RA (McInnes & Schett, 2011). Selain itu, merokok juga meningkatkan ACPA seseorang karena rokok memiliki berbagai senyawa ROS (radical oxygen species). ACPA bisa berasal dari isotipe IgG, IgA, atau IgM. ACPA sendiri bisa memiliki sifat patogen, dengan mengaktifkan makrofag (via TLR atau berinteraksi dengan reseptor Fc) atau mengaktifkan osteoklas via pembentukan kompleks imun, sehingga dapat meningkatkan bone loss (Smolen et al., 2016).
Seperti yang kita tahu, RA disebabkan oleh adanya inflamasi di sendi dan beberapa organ lain sehingga sendi tersebut menjadi inaktif dan kaku. Inflamasi pada RA sendiri dapat melalui tiga pathway: pathway sistem imun adaptif, pathway sistem imun innate, dan pathway sitokun (McInnes & Schett, 2011). Membran sinovial pada penderita RA memiliki sel myeloid dan sel plasmasitoid yang melimpah. Kedua sel tersebut mensekresikan berbagai macam sitokin (interleukin-12, 15, 18), HLA kelas II, dan molekul-molekul konstimulasi yang penting bagi aktivasi sel T dan pengenalan antigen. Umumnya, progresi RA dimediasi oleh sel T helper tipe 1 dan tipe 17 (McInnes & Schett, 2011). Sel T yang terdapat di sekitar membran sinovium dapat menjadi autoreaktif karena adanya self-protein yang tersitrulinasi. Sel T helper tipe 1 dan 17 inilah yang menjadi autoreaktif. Selain itu, sel T helper juga dapat diaktivasi oleh beberapa interleukin seperti interleukin 6, 21, dan 23. Selain mengaktifkan sel T helper, tiga interleukin yang disebutkan sebelumnya dapat menonaktifkan sel T regulator yang berperan penting dalam mengontrol aktivitas srl T (McInnes & Schett, 2011).. Meningkatnya interleukin 6, 21, dan 23 tersebut disebabkan karena faktor genetik dan epigenetik.
Selain karena autoimun sistem imun selular, sistem imun humoral juga berperan penting dalam progresi RA. Di dalam sinovium sering dijumpai adanya sel plasmablast dan sel plasma. Sel B CD20+ diketahui memiliki efek yang cukup signifikan pada progresi RA karena mampu menghasilkan ACPA dan RF yang merupakan autoantibodi serta dapat menginduksi sistem komplemen (McInnes & Schett, 2011).
Pathway sistem imun innate melibatkan berbagai macam sel seperti makrofag, sel mast, neutrofil dan sel NK yang ada di membran sinovial. Terdapat faktor utama yang menyebabkan influks masif sel-sel imun innate ke dalam membran sinovial. Faktor-faktor tersebut disingkat dengan GM-CSF, yaitu granulocyte-macrophage colony-stimulating factor. GM-CSF menyebabkan maturasi sel-sel sistem imun dan mendorong terjadinya influks besar-besaran dari pembuluh darah terdekat (McInnes et al., 2011). Peran makrofag pada pathway ini sangatlah penting. Makrofag mampu melepas sitokin seperti TNF-α, interleuikin-1, 6, 12, 15, 18, dan 23; ROS, dan enzim pendegradasi matriks (McInnes & Schett 2011). Sitokin-sitokin tersebut juga disebut sebagai pro-inflamatory cytokine.
Sitokin berperan meningkatkan inflamasi di sekitar sinovium dengan cara melepaskan prostaglandin, protease, dan ROS. Sel Mast berperan dalam memproduksi amina vasoaktif, sitokun, kemokin, reseptor Fc dan ST2. Beberapa ACPA dapat meningkatkan kinerja sel Mast dalam melepaskan senyawa-senyawa pro-inflamatory (McInnes & Schett. 2011). Selain menarik sel-sel imun, kemokin dan sitokin yang dilepaskan oleh berbagai komponen sistem imun juga akan mengaktifkan sel-sel endotel sinovium sehingga ia akan melepaskan lagi sitokin dan kemokin yang lebih banyak (Smolen et al., 2016).
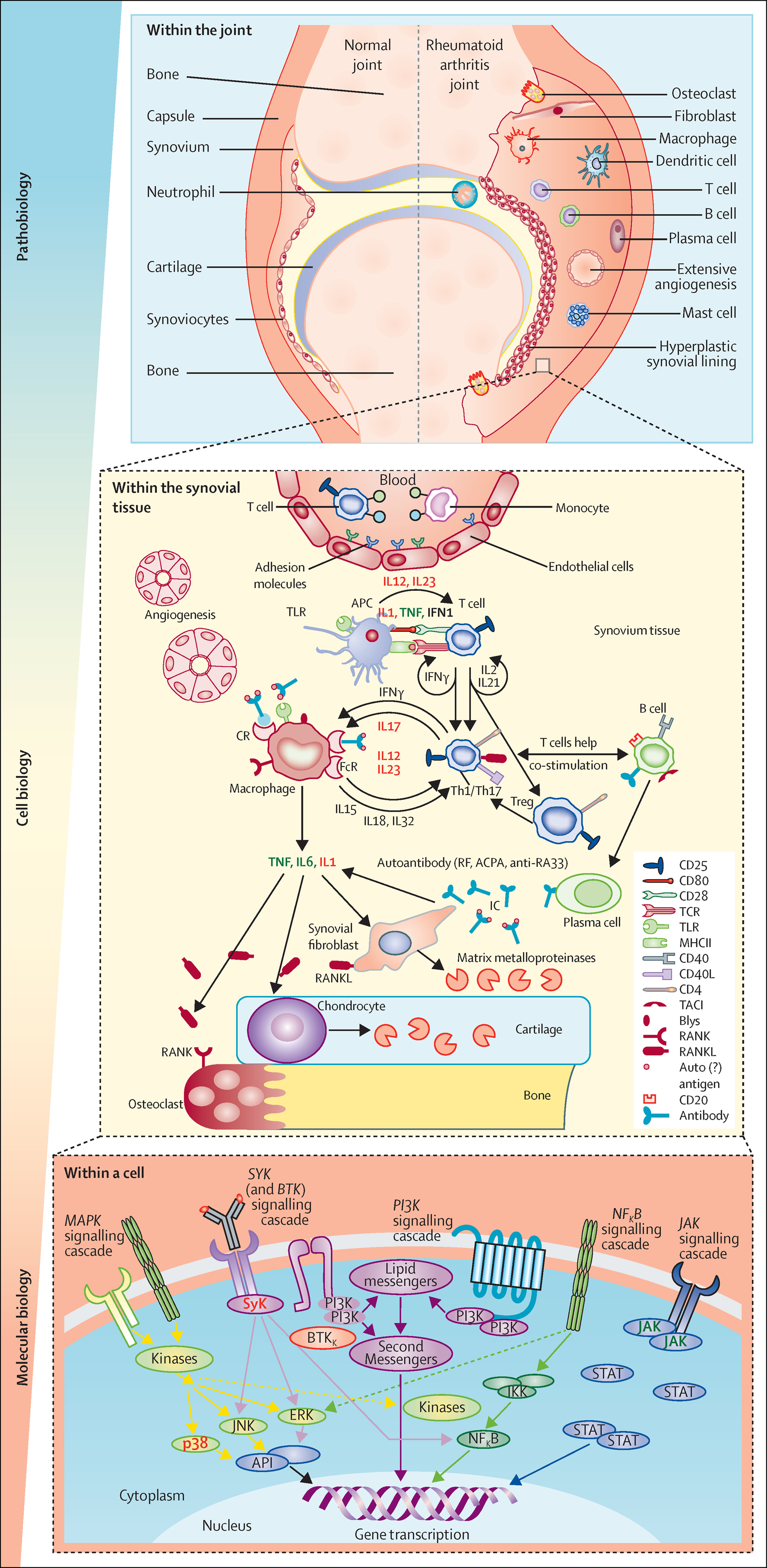
Gambar 4 Interaksi selular pada patofisiologi dan patogenesis RA (Smolen et al., 2016)
Monosit, makrofag, sel T, sel B, dan fibroblas yang teraktivasi karena sitokin dan kemokin (Gambar 4) akan memicu pembentukan osteoklas (sel pengikis sel tulang) melalui RANKL yang diekspresikan pada sel T dan sel B. Reseptor RANKL terdapat pada sel dendritik, sel makrofag, dan sel preosteoklas (Smolen et al., 2016). Adanya interaksi RANKL-reseptor RANK akan mempercepat maturasi preosteoklas menjadi osteoklas yang dapat mengerosi jaringan tulang di daerah sinovial dan persendian. Osteoklas memiliki enzin asam yang dapat menghancurkan mineral-mineral yang terdapat di tulang rawan persendian. Secara lebih rinci, patofisiologi dan patogenesis RA dapat dilihat pada Gambar 4.
III. Treatment dan Obat Artritis Reumatoid
Sebagian besar obat dan mekanisme terapi RA merupakan inhibitor sitokin. TNF-α adalah target populer dari obat-obatan yang menginhibisi sitokin. Adalimumab, certolizumab, pegol, etanercept, golimumab, dan infliximab adalah jenis obat inhibitor sitokin yang menarget TNF-α (McInnes & Schett, 2011). Seperti yang telah dijelaskan di atas, TNF-α memiliki peran utama dalam mengaktifkan sel-sel sistem imun dan endotel sehingga mereka meningkatkan ekspresi berbagai macam sitokin dan kemokin yang turut serta meningkatkan progresi RA. Selain itu, aktivasi fibroblas dan supresi sel T regulator juga dimediasi oleh TNF-α (McInnes & Schett, 2011).
Selain TNF-α, interleukin 6 juga merupakan target populer sebab interleukin-6 mengaktifkan leukosit dan meingkatkan produksi antibodi, terutama autoantibodi seperti ACPAA dan RF. Tocilizumab adalah salah satu contoh jenis obat inhibitor sitokin yang menarget interleukin 6. Selain itu, CD20 juga merupakan target dari salah satu obat RA, seperti Rituximab (McInnes & Schett, 2011). CD20 mampu mengkativasi fibroblas, makrofag, dan menginduksi sel plasma untuk memroduksi ACPA.
IV. Kesimpulan
Artritis reumatoid merupakan penyakit autoimun yang melibatkan berbagai macam komponen sistem imun. RA diawali dengan peningkatan abnormal ACPA, sebuah autoantibodi yang dapat menyerang self-protein dan protein-protein terstrulinasi lainnya. Protei tersitrulinasi mengalami perubahan struktur sehingga dianggap sebagai antigen. Peningkatan kadar ACPA ini disebabkan oleh faktor genetik, epigenetik, dan lingkungan (seperti merokok dan peruahan struktur mikrobioma). Selain itu, beberapa interleuikin juga dilepaskan sebagai akibat dari interaksi ACPA dengan sel-sel sistem imun. Interleukin tersebut mampu mengkativasi sel T helper dan menonaktifkan sel T regulator sehingga kerja sel T pun tidak terkontrol. Faktor-faktor yang dilepas makrofag seperti GM-CSF dapat menarik berbagai jenis sel-sel sistem imun innate ke dalam membran sinovial. Sel T dan Sel B yang telah teraktivasi dapat membentuk RANKL yang menyebabkan terbentuknya osteoklas. Osteoklas dapat menyebabkan erosi dan pengikisan mineral di jaringan tulang rawan sendi. Obat yang mampu menyebuhkan RA antara lain menarget sitokin dan kemokin penting seperti TNF-alfa dan interleukin 6.
V. Daftar Pustaka
CDC. (2018). Rheumatoid Arthritis (RA). Retrieved from Center for Disease Control and Prevention site https://www.cdc.gov/arthritis/basics/rheumatoid-arthritis.html [10 Desember 2018]
McInnes, I. B., & Schett, G. (2011). The pathogenesis of rheumatoid arthritis. New England Journal of Medicine, 365(23), 2205-2219.
Raptopoulou A, Sidiropoulos P, Katsouraki M, Boumpas DT (2007). Anti-citrulline antibodies in the diagnosis and prognosis of rheumatoid arthritis: evolving concepts. Crit Rev Clin Lab Sci. 44 (4): 339–63.
Shah, Ankur (2012). Harrison’s Principles of Internal Medicine (18th ed.). United States: McGraw Hill.
Smolen, J. S., Aletaha, D., & McInnes, I. B. (2016). Rheumatoid arthritis. The Lancet, 388(10055), 2023–2038. doi:10.1016/s0140-6736(16)30173-8
WHO (2018). Disease and injury country estimates. Retrieved from Health statistics and information systems, World Health Organization https://www.who.int/healthinfo/global_burden_disease/estimates_country/en/ [11 Desember 2018]
